Fundamentos de la química
¿Qué es la química?
La química es la ciencia que nos ayuda a entender de qué están hechas las cosas y cómo cambian. Todo lo que ves, tocas o incluso respiras está hecho de algo llamado "materia", y la química estudia cómo se comporta esa materia.
Ejemplo: La química explica por qué el hielo se derrite o cómo el jugo de limón puede limpiar una moneda oxidada.
Propiedades de la materia
Las propiedades son las cosas que caracterizan/identifican a algo, en este caso, a la materia. Como se dijo anteriormente, la materia es todo lo que ocupa espacio y tiene peso. ¡Incluso el aire es materia!
Ejemplo: células, animales, planetas, personas, fuego, etc.
- Propiedades físicas: Cómo se ve o siente algo (color, tamaño, forma, textura).
- Propiedades químicas: Cómo algo puede transformarse en otra cosa (por ejemplo, la madera quemándose se convierte en ceniza).
Ejemplo: El agua es líquida (propiedad física), pero si hierve, se convierte en vapor, y si se congela, se hace hielo (propiedades químicas).
Cambios físicos y químicos
- Cambio físico: La materia cambia de forma, pero sigue siendo la misma. Ejemplo: cortar papel o derretir hielo.
- Cambio químico: La materia se transforma en algo completamente nuevo. Ejemplo: quemar papel o cocinar un huevo.
 El papel no deja de ser papel aunque se haya roto.
El papel no deja de ser papel aunque se haya roto.

Pista clave: Si no puedes volver atrás, probablemente fue un cambio químico. En el caso de arriba, el huevo frito no volverá a ser un huevo normal.
Unidades y mediciones
Para medir cosas en química utilizamos el Sistema de Unidades, el cual no es más que un conjunto de medidas estándar que se utilizan para medir cosas. Algunos ejemplos son:
- Longitud: Esta magnitud utiliza los metros (m)
- Peso: Esta magnitud utiliza los kilogramos (kg)
- Volumen: Esta magnitud utiliza los litros (L)
- Temperatura: Esta magnitud utiliza los grados Celsius (°C) o Kelvin (K).
Nota: Es de suma importancia anotar la magnitud y no confundirse. Por ejemplo:
"He recorrido 30". Al no especificar la magnitud, no sabemos cuánto recorrió.
"He recorrido 30 kg". En este caso podemos apreciar que se ha utilizado mal la magnitud, al ser corregida debería decir "He recorrido 30 m".
Cifras significativas
Esto es para ser precisos cuando medimos cosas. No escribimos "infinidad" de números, solo los necesarios para que los datos sean claros y útiles.
Ejemplo: Si tu regla mide hasta milímetros, decir que algo mide 3.45 cm está bien, pero decir 3.45678 cm no tiene sentido porque no puedes medir tan exacto.
Estructura atómica
Todo está hecho de átomos, absolutamente todo, las personas, los insectos, bacterias, ¡Hasta las celulas! Los átomos son como pequeños ladrillos invisibles que forman la materia.
Partes del átomo:
- Protones: Son particulas que se encuentran en el núcleo del atomo. Tienen carga positiva (+)
- Neutrones: Son particulas que se encuentran en el núcleo del atomo. Tienen carga neutra
- Electrones: Son particulas que están alrededor del átomo. Tienen carga negativa (-)
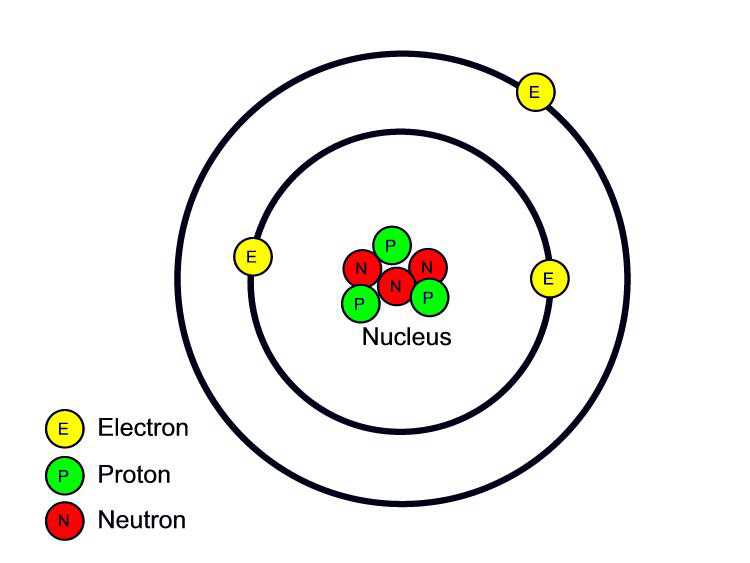 Átomo de Litio.
Átomo de Litio.
Número atómico y masa atómica
- Número atómico: Dice cuántos protones tiene un átomo. Esto lo hace único. Por ejemplo, el hidrógeno siempre tiene 1 protón, así que su número atómico es 1.
- Masa atómica: Suma total de protones y neutrones en el núcleo. Se puede calcular utilizando la siguiente fórmula:
A = p + n
A = Masa átomica
p = Número de protones
n = Número de neutrones
Ejemplo: El helio tiene 2 protones y 2 neutrones.
A = p + n
A = 2 + 2
A = 4
Por ende, la masa atómica del helio es igual a 4.
Modelos atómicos
A lo largo de la historia ha habido varias formas para representar a los átomos, entres las principales están:
- Modelo de Dalton (1803): Imagina el átomo como una pequeña esfera indivisible, como una canica. Dalton dijo que cada elemento está formado por átomos de un tipo específico, y esos átomos se combinan para formar compuestos.
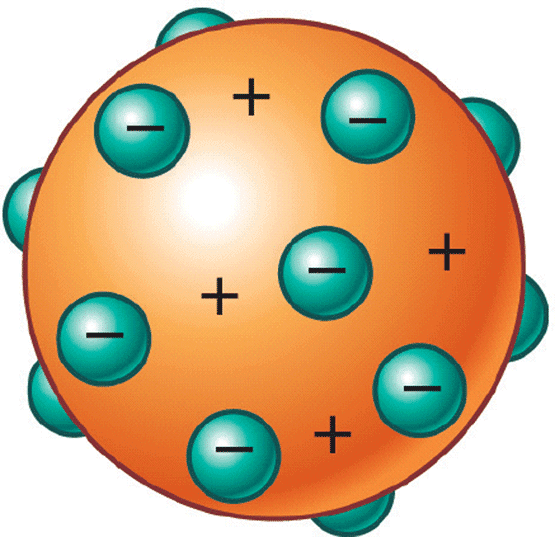
Modelo de Thomson (1897): Este modelo es como una "pudín de pasas". Los átomos son esferas con carga positiva, y los electrones (cargas negativas) están distribuidos dentro de ellas, como pasas en un pudín.
- Modelo de Rutherford (1911): Rutherford descubrió que el átomo tiene un núcleo pequeño y denso en el centro (con carga positiva), mientras que los electrones giran alrededor de él, como planetas alrededor del sol.
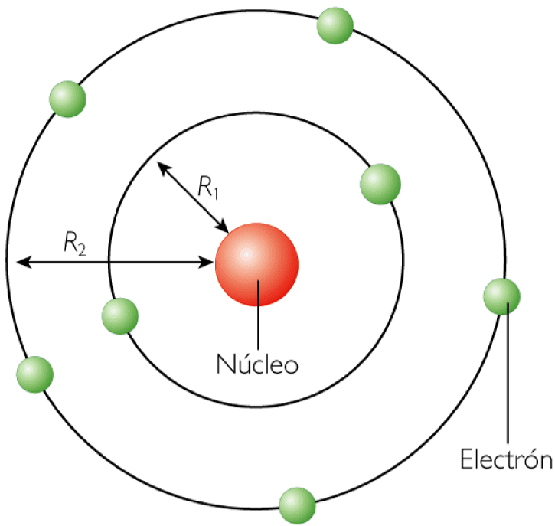
- Modelo de Bohr (1913): Bohr propuso que los electrones se mueven en órbitas fijas alrededor del núcleo, y cada órbita tiene una energía específica. Cuando un electrón se mueve entre órbitas, emite o absorbe luz.
- Modelo cuántico ondulatorio (1926): Este modelo es más complejo. Los electrones no siguen trayectorias fijas. En lugar de eso, se describen en "nubes" o áreas de probabilidad donde es más probable encontrar un electrón. Estas áreas se llaman orbitales.